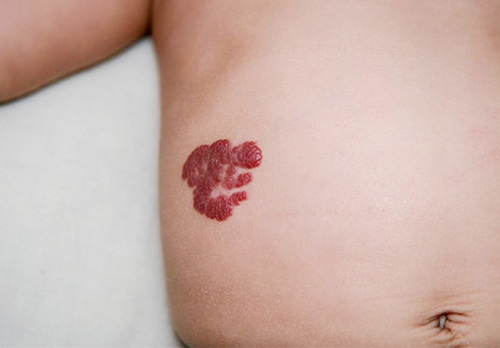
Инфантильная гемангиома (далее ИГ) — доброкачественная опухоль, часто возникающая у детей первого года жизни, в основе которой лежит пролиферация клеток эндотелия сосудистого русла.
Эпидемиология
Возникает у 4-5% новорожденных; чаще поражает женский пол в соотношении 5:1. Последние исследования свидетельствуют о более частом возникновении ИГ среди новорожденных Кавказской национальности, по сравнению с остальными расами. Считается, что с большей частотой возникает у новорожденных с неблагоприятным акушерским анамнезом или осложнениями в родах: возраст матери больше 40 лет, недоношенность, ЗВУР, внутриутробная гипоксия и т.д. Чаще всего возникает спорадически, однако есть данные по семейным случаям возникновения ИГ-предполагают аутосомно-доминантное наследование, однако специфические гены, отвечающие за данную патологию, пока не выявлены.
Патогенез
Существует множество теорий развития данной аномалии. Ведущей в настоящее время является теория гипоксического стресса, согласно которой, механическое давление в родах, на ту или иную область, в совокупности с генерализованной гипоксией в родах, приводит к индуцированию синтеза проангиогенных факторов: GLUT 1 (глюкозный транспортер тип 1), VEGF (фактор роста эндотелия сосудов), βFGF (фактор роста фибробластов). Последние, в свою очередь, активируют эндотелиальную клетку предшественницу и запускают процесс неконтролируемой пролиферации, что приводит к образованию опухоли. Интересный факт, что данная клетка предшественница позитивна по антигенам (далее-АГ) CD133 и CD13. Данные гликопротеины находятся на поверхностях многих клеток, как «нормальных», так и онкологически измененных. Существуют исследования касательно разработки вакцин против опухолей типа меланомы, клетки которой, также обладают данными антигенами. Другая теория, свидетельствует о том, что исходной материнской клеткой гемангиомы являются клетки трофобласта плаценты, которые были занесены в ту или иную область кровеносного русла в течение развития плода или процесса родов. И последняя теория предполагает образование инфантильной гемангиомы путем васкулогенеза denovo из материнской клетки предшественницы, подвергшейся мутации генетического материала, или же образование новых сосудов из уже существующей капиллярной сети, в клетках которой произошла мутация.
Клинические проявления
ИГ отсутствуют при рождении. Это основная дифференциальная диагностика с сосудистыми мальформациями. Однако, при рождении, место поражения может быть представлено областью побледнения- вазоконстрикции, эритематозным пятном, телеангиэктазией или образованием, напоминающим гематому. Локализация абсолютно повсеместна, как на коже, так и на слизистых оболочках. Но с наибольшей частотой они появляются в области головы и шеи (60% случаев). Далее в порядке убывания: туловище (25% случаев), конечности (15% случаев).
Существует обширная классификация гемангиом. Однако ее стоит рассматривать в совокупности с клиническими проявлениями данной патологии. Гемангиомы бывают поверхностные , глубокие и смешанные. Поверхностные захватывают эпидермис и поверхностные слои дермы и представляют собой узлы или бляшки ярко красного цвета, с гладкой или рельефной поверхностью, при надавливании бледнеют, но не исчезают. Глубокие гемангиомы представляют собой образования, эластичной консистенции, залегающее в глубине мягких тканей, цвет кожных покровов над этим образованием или не изменен, или имеет голубой оттенок с телеангиэктазиями. Смешанные содержат в себе признаки как поверхностных, так и глубоких гемангиом.
Также ИГ бывают локализованными (нодулярными) и распространенными (сегмантарными). Локализованные представляют собой классические формы, так называемые «strawberry marks»; распространённые встречаются реже, их течение и прогноз хуже, чем у локализованных форм. Представляют собой бляшковидные структуры, ассоциированные с другими висцеральными и сосудистыми аномалиями, формируя целые синдромы: PHACES-синдром (Рис.3), (Posterior fosse abnormalities-мальформации задней черепной ямки-синдром Дэнди-Вокера, Hemangioma-гигантская гемангиома лица, захватывающая все 4 сегмента (Рис.4), Arteriesanomalies-церебро-васкулярные артериальные аномалии, Coarctationaortic-коарктация аорты и другие сердечно-сосудистые аномалии, сопряженные с развитием сердечно-сосудистой недостаточности, Eyestroubles-окулярные мальформации/Sternalmalformations-дефекты грудины/белой линии живота); синдром LUMBAR (Lower body hemangiomas-врожденные гемангиомы, липомы и другие образования нижней части тела, Urogenital malformations-урогенитальные мальформации и изъязвления, Myelopathy-миелопатия, Bonedeformation костные деформации, Anorectal Arterial troubles-аноректальные и артериальные аномалии, Renal anomalies-аномалии почек); PELVIS синдром (Perineal angioma-Перинеальная гигантская гемангиома, External genital malformation-экстрагенитальные мальформации, Lipomyelomeningocel- липомиеломенингоцеле, Vesicorenal abnormalities- аномалии почек и мочевого пузыря, Imperforate anus- атрезия ануса, Skin tag-акрохордоны); SACRAL синдром (Spinal dysraphism-спинальный дизрафизм, Anogenital, Cutaneous, Renal and urologic malformation-аногенитальные, кожные, почечные и урогенитальные аномалии, Angioma Lombosacral-гемангиома кресцовокопчиковой области).
Гистология
В течение своего роста и развития, гемангиомы преодолевают несколько стадий, в процессе которых меняются как клинические проявления, так и гистология данных образований. Чаще всего ИГ возникают в первые 1-4 недели жизни новорожденного и вступают в первую фазу своего развития-рост. Рост представляет собой усиленную пролиферацию клеток эндотелия и длится от 3-х до 9-ти месяцев. Гистологически на данном этапе ИГ представляет собой узел, питаемой немногочисленными артериолами, представляющий собой скопление гиперплазированных эндотелиальных клеток и перицитов, с или без базальной мембраны и наличием сосудистых просветов. К первому году жизни гемангиома переходит в стадию стабилизации (плато) с последующей самопроизвольной инволюцией, продолжающейся от 3 до 7 лет. Гистологически узел претерпевает изменения: просветы становятся шире, эндотелиоциты сплющиваются, в результате чего узел приобретает дольчатое строение, начинается фиброз, с постепенным полным замещением узла соединительной тканью. Именно с этим связано возникновение остаточных явлений в виде рубцов. С биохимической точки зрения, запуск фиброза ассоциирован с выработкой тканевых ингибиторов ангиогенеза-металлопротеиназ.
Осложнения
Тактика ведения пациентов с ИГ и прогноз сильно зависит от места локализации данной аномалии. Подавляющее большинство проходят практически бесследно, оставляя небольшой косметический дефект в виде рубца. Тактика ведения таких форм сводится к динамическому наблюдению. В 10-20% случаев ИГ могут быть причиной серьезных осложнений, вплоть до возникновения жизнеугрожающих состояний. Такие формы нуждаются в обязательной безотлагательной терапии. Осложнения ИГ условно можно разделить на несколько групп:
- ИГ с риском витальных осложнений. В данную группу относятся: гемангиомы подглоточного пространства, которые могут приводить к респираторному дистресс-синдрому (клинически проявляетс стридором и ларингеальной отдышкой); гигантские гемангиомы, ассоциированные с поражением других органов и систем, например упоминавшийся ранее PHACES-синдром; ИГ желудочно-кишечного тракта с риском изъязвления/травматизации и развития желудочно-кишечного кровотечения; ИГ в количестве 5 и более, расположенных на нескольких анатомических областях-риск наличия гемангиом печени.
- ИГ с риском развития функциональных расстройств. В эту группу входят гемангиомы с высоким риском осложнений в виде некрозов, изъязвлений, вторичного инфицирования, кровотечения, а также развитие эстетических нарушений. Такие ИГ имеют крайне специфическую локализацию: окулярная/пальпебральная/внутриорбитальная/ретроорбитальная-высокий риск повреждения структур глаза, вплоть до полной утраты его функции; лабиальная-поражение губ в первую очередь приводит к расстройству акта сосания и слюнотечению; назальная-обтурация воздухоносных путей, сюда же относятся гемангиомы Сирано (кончика носа), возникновение которых, сопряжено с выраженными косметическими дефектами и возможным вторичным разрушением хрящей носа; аурикальная-разрушение хрящевых структур с возможной потерей слуха; околоушная область-поражение лицевого нерва; перинеальная-анатомический дефект с нарушением акта дефекации и микции; сакральная область-при вовлечении в патологический процесс спинного мозга-парез нижних конечностей и расстройство тазовых функций; околососковая область-асимметрия грудной клетки с возможным нарушением строения и развития молочных желез; область кисти или стопы-нарушение двигательных функций; области естественных складок.
- ИГ с риском развития эстетических осложнений-большие размеры гемангиом с локализацией на лице, носу губах, веках-в исходе, в следствие обширного поражения эпидермиса и выраженного фиброза в стадию инволюции, кожа приобретает атрофические и рубцовые изменения. Кроме последних, остаточные явления также могут быть представлены телеангиэктазиями и фиброзно-жировыми изменениями.
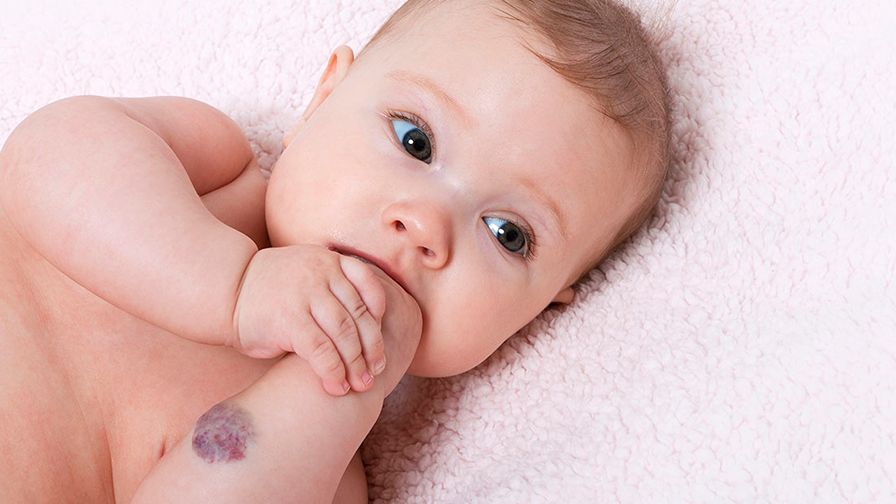
Внимание! Новый сервис!
В нашем Центре открыт Кабинет диагностики и лечения инфантильных гемангиом
Диагностика
Диагностика поверхностных форм, чаще всего, проводится на основании клинических проявлений и физикального осмотра. Биопсия с гистологическим и иммуногистохимическим исследованиями, проводится при наличии сомнений в постановке диагноза и при дифференциальной диагностике с сосудистыми мальформациями и злокачественными образованиями (чаще единичные, с плотной структурой, деформирующей рельеф кожи). Для диагностики глубоких форм гемангиом, используются: ультразвуковое исследование, КТ и МРТ-чаще для определения глубины поражения и залегания образования.
Терапия
Как уже упоминалось ранее, в 80-90% случаев, тактика ведения пациентов с гемангиомами сводится к наблюдению и бездействию. Для остальных случаев разработан протокол лечения, включающий в себя консервативные и хирургические методы.
Консервативная терапия:
- Глюкортикостероиды системные и местные-эффективны, однако большие дозировки (2-5 мг/кг/сут) приводят к обширным побочным эффектам: вторичный синдром Кушинга, нарушение сна, ГЭРБ, акне, остеопороз, артериальная гипертензия, вторичная иммуносупрессия, задержка физ. развития, надпочечниковая недостаточность, эрозии ЖКТ и т.д; Длительность лечения: ударные дозы в течение 2-х месяцев, далее постепенное снижение доз в течение месяца во избежание синдрома отмены.
- Интерферон-a-2а и интерферон-a-2b-мощный антиангиогенный эффект за счетингибирования фактора роста фибробластов (FGF). Доза составляет от 1 до 3 млн ЕД/м2 / сут подкожно. Терапия длительная: от 6 до 12 мес. Однако терапия сопровождается мощными побочными эффектами: псевдогриппозный синдром (температура, мышечные боли), гемотоксичность (нейтропения), гепатотоксичность (повышение трансаминаз), депрессивный синдром, нейротоксичность (вплоть до задержки физического развития). Противопоказаны детям до 1 года;
- Винкристин-химиопрепарат, вызывающий апоптоз пролиферирующих клеток. Применяется при осложненных и висцеральных формах ИГ. Доза 0,05 мг/кг или 1 мг/м2 внутривенно 1 раз в неделю. Длительность терапии 15-24 нед. Но, также как и предыдущих средств, имеет выраженные побочные эффекты: алопеция, запоры, боли, полинейропатия, гемотоксичность (нейтропения);
- Неселективные β-адреноблокаторы-пропранолол-в настоящее время-«золотой стандарт» лечения ИГ. Механизм действия пока до конца не изучен. Предполагается несколько вариантов: 1-Периферическая вазоконстрикция с уменьшением кровотока в опухоли за счет непосредственного блокирования β2 -адренорецепторов и подавления экспрессии NO-синтетазы в ткани опухоли, что приводит к снижению синтеза NO (стимулятор продукции проангиогенных факторов роста). 2-Антиангиогенный эффект за счет: блокирования проангиогеных факторов; ингибирования ERK-сигнального пути (путь запуска пролиферации и выживаемости клеток через синтез сигнальных белков VEGF и βFGF, являющимися сильными индукторами ангиогенеза); блокирование синтеза металлопротеиназ, участвующих в синтезе цитоскелета клетки, что приводит к торможению роста опухоли. 3-Индукция апоптоза-через уменьшение концентрации VEGF и прямого влияния на β2 -адренорецепторы. Данная терапия хорошо себя зарекомендовала и за счет небольшого количества побочных эффектов, по сравнению с вышеизложенными препаратами: бронхоспазм (противопоказаны пациентам с астмой в анамнезе), расстройства ЖКТ, асимптоматическая артериальная гипотензия, риск развития гипогликемии, нарушения ритма, нарушения сна, сыпь. С большой осторожностью необходимо рассматривать назначения данных препаратов при PHACE-синдроме, так как наличие обширных цереброваскулярных аномалий может привести к снижению мозгового кровотока и усугублению ишемии. Стандартная доза 2-3 мг/кг/сут-3 раза в сутки каждые 6 часов. Целевая доза достигается постепенно, начиная со стартовой 0,5-1 мг/кг/сут. Отмена также постепенна-в течение 2-3 недель (Резкое прекращение приема может привести к рецидиву). Продолжительность терапии от 3 до 12 месяцев (рекомендовано не менее 6 мес). Перед назначением необходимо провести тщательным сбор анамнеза, на предмет наличия сердечно-сосудистых заболеваний, а также провести объективный осмотр и инструментальное обследование (ЭКГ, ЭхКГ, холтеровское мониторирование). Крайне редко наблюдается резистентность к проводимой терапии, которая преодолевается увеличением дозировки до 3-4 мг/кг/сут.
- Селективный β1 -адреноблокатор-атенолол. Эффективность данного средства в настоящий момент находится на стадии изучения. Из-за отсутствия воздействия на β2 -адренорецепторы, отсутствует влияние на легкие, поджелудочную железу, снижая риски гипогликемии и бронхоспазма.
- Топические формы β-адреноблокаторов-тимолол. Метаанализ исследований свидетельствует о высокой эффективности и безопасности данных форм. Однако единых рекомендаций по применению препаратов пока нет.
Хирургическое лечение:
- Показания: –рано развившийся некроз мягких тканей; – грубые функциональные расстройства со стороны органов зрения и слуха; – остаточные проявления (персистенция резидуального объема после инволюции); – деформация анатомических структур.
- Лазер эффективен только в отношении поверхностных форм ИГ. Применяется для коррекции косметических дефектов постинволюционной стадии.
- Криотерапия-эффективен только в отношении поверхностных форм. Требует неоднократного применения. Процедура болезненная, лечение проводится под общей анестезией. Может приводить к локальным осложнениям: развитию некрозов, изъязвлений с вторичным инфицированием. В настоящее время практически не используется.
Список литературы:
- Л.А. Хачатрян, Д.М. Николаева; Современная терапия инфантильных гемангиом; Вопросы гематологии/онкологии и иммунопатологии в педиатрии; 2021; 20 (2): 156–167
- Amal Chamli; Payal Aggarwal; Radia T. Jamil; Noureddine Litaiem; Hemangioma; StatPearls Publishing LLC; Review; 2021 July
- Haggestrom A.N, Lammer E.J, Schneider R.A et al. Patterns of infantile hemangiomas: new clues
to hemangioma patogenesis and embryonic facial development; Pediatrics; 2006; 117 698-703 - Hemangioma Investigator Group; Prospective study of infantile hemangiomas:
demographic, prenatal and perinatal charasterics; The Journal of Pediatrics; 2007; 150(3) 291-294 - Leaute-Labreze C, Prey S, Ezzedine K.; Infantile hemangioma part 1.
Pathophysiology, epidemiology, clinical features, life cycle and associated
structural abnormalities. The Journal of the European Academy of Dermatology and Venereology; 2011; 25(11) 1245-1253 - Tina S. Chen, Lawrence F; Infantile Hemangiomas: An Update on Pathogenesis and Therapy;
Pediatrics; January 2013; 131 (1): 99-108
